Biosseguridade, Frangos de Corte, Outras doenças, Postura Comercial
Baseado nos avanços das técnicas de diagnósticos, podemos afirmar que a APEC é uma zoonose?

A Colibacilose nos últimos anos tem sido um problema muito significativo para a indústria Avícola brasileira. Seus impactos vão muito além de mortalidade inicial de pintinhos, os danos são sentidos em toda a cadeia produtiva e o que mais vem impactando, são as condenas em abatedouros por Aerossaculite.
De maneira geral, os problemas gerados por esse agente podem ser tanto primários como secundários, e com o avanço de técnicas moleculares nos últimos 10 anos, essa afirmação pode ser evidenciada em vários artigos científicos.
Uma compreensão completa do patótipo de APEC (Avian Pathogenic E coli) permaneceu elusiva, e em partes devido à grande diversidade genética das populações bacterianas e estratégias inadequadas de diagnóstico e tipagem (Ronco et al., 2017). Além disso, a APEC tem sido relacionada como um risco zoonótico devido a alta similaridade genética entre certos isolados de APEC e (UPEC) infecções do trato urinário em humanos (Maluta et al., 2014).
Nesse sentido, o sequenciamento de genoma inteiro (WGS) tem o potencial de informar sobre a filogenia, dinâmica populacional e epidemiologia molecular de E. coli de diferentes origens e nichos, podendo ser a base para uma melhor definição de patótipos ainda não esclarecidos, e não ficando somente na classificação da sorotipagem. Estima-se que a 80% das APEC pertencem aos sorogrupos O1, 02 e O78 (Huja et al., 2015). Outra forma de avaliar o potencial patogênico das APEC é através da virulotipagem, ou identificação de genes de patogenicidade presentes no seu material genético, embora eficazes para detecção, esses métodos consideram que não há fator únicos ou combinações de determinantes associados a todas as cepas de APEC (Azam et al., 2019).
O genoma das cepas de E. coli sofre frequentes aquisições, deleções e eventos de recombinação em resposta à pressão seletiva ecológica, resultando em uma diversidade muito grande de material genético. Consequentemente, a classificação proposta por Clermont et al., 2019, determina até o momento 9 filogrupos:
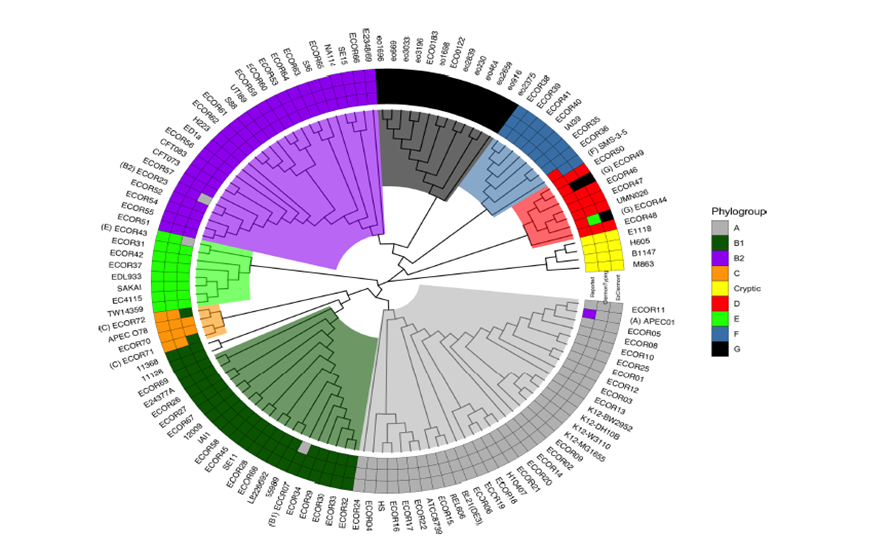
Em última análise, os dados do WGS mostram que os marcadores de sorotipo são insuficientes para detectar e diferenciar com precisão as linhagens de APEC. A aparente capacidade das linhagens APEC predominantes em colonizar múltiplos hospedeiros destaca o fato de que existem semelhanças nos fatores que determinam a infecção extra-intestinal entre diferentes hospedeiros animais e indica a ameaça zoonótica representada por esses genótipos.
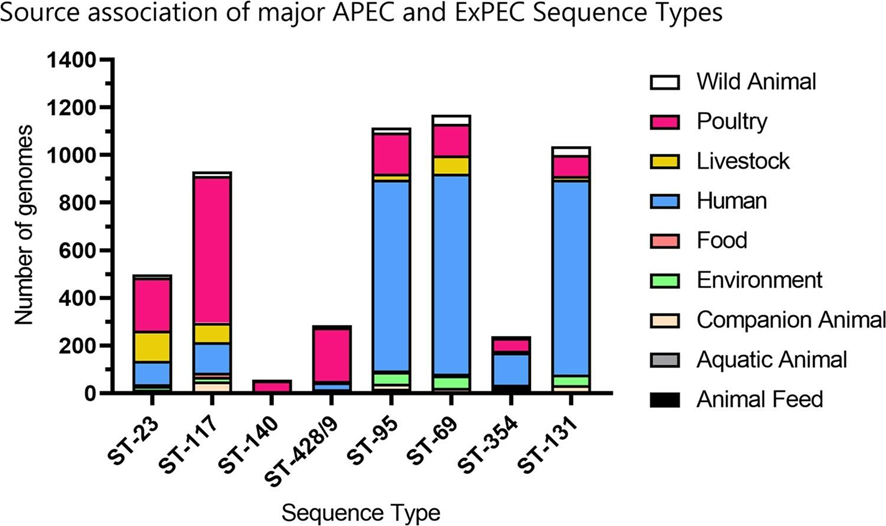
Fonte: Mehat et al., 2021
APEC são frequentemente citados como potenciais patógenos zoonóticos devido à alta semelhança de certas cepas de APEC com isolados de UPEC/ExPEC implicados em doenças humanas (Logue et al ., 2017 ; Khairy et al ., 2019 ; Jørgensen et al ., 2019 ). A colonização de nichos extra-intestinais necessita de adaptações bacterianas específicas, que muitas vezes são conferidas a APEC e ExPEC por determinantes de virulência. Dado que esses requisitos de nicho são semelhantes entre as espécies animais, são esperadas semelhanças nos determinantes de virulência entre ExPEC causando doenças em diferentes hospedeiros animais (Singer, 2015). Isso é especialmente verdadeiro quando os sorotipos e fatores de virulência esperados codificados pela APEC são reduzidos a um conjunto minimamente preditivo (Johnson et al., 2008 ).
Embora a alta similaridade genética sugira potencial zoonótico, a transmissão de APEC de aves para um hospedeiro humano não foi demonstrada. Supõe-se que a transmissão seja indireta através do consumo de produtos avícolas de varejo que posteriormente causam infecções urinárias transmitidas por alimentos (Liu et al., 2018 ; Saidenberg et al ., 2020 ).
WGS tem o potencial de elucidar se existem quaisquer sinais genéticos associados à adaptação ao hospedeiro em genótipos multi-hospedeiros (O'Boyle et al ., 2020), permitindo assim que o aspecto zoonótico da APEC seja investigado com mais detalhes. Os dados WGS para outros patógenos bacterianos foram usados para inferir a história evolutiva e examinar a frequência e o tempo de eventos de mudança de hospedeiro multidirecional (Richardson et al ., 2018 ).
Conheça nossas soluções de imunoprofilaxia para Colibacilose em aves.
https://www2.zoetis.com.br/especies/aves/
Autor:
Gleidson Salles – M.V. MSc Serviços Técnicos | Zoetis – Aves

Gleidson Salles
PRECISA DE MAIS INFORMAÇÕES A RESPEITO DESSE TEMA?
Fale com a nossa equipe técnica!














